+
订阅
美国FDA批准两款更新版COVID-19加强针
更新于2023-09-12 16:02
北美商业电讯
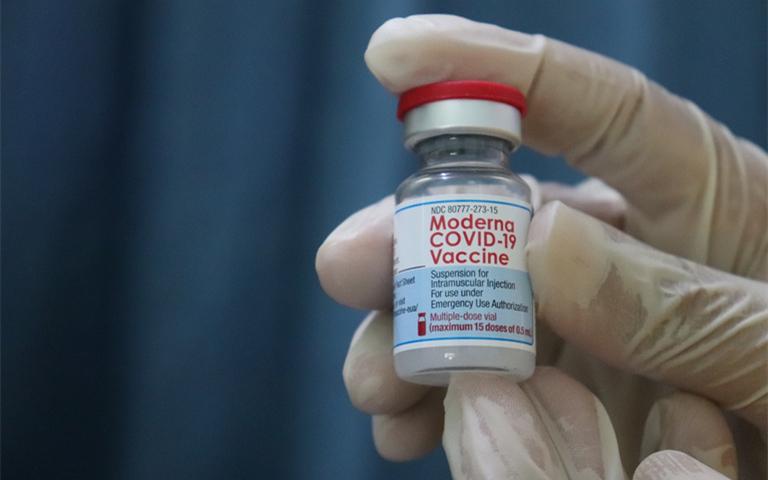
周一,美国食品药品监督管理局(FDA) 批准了辉瑞/BioNTech 和莫德纳公司的新型COVID-19强化疫苗,以对抗仍在传播的新冠病毒。
值得注意的是,除了上述两款,诺瓦瓦克斯医药公司(Novavax)生产的第三款疫苗此次并未获批,仍在接受FDA的审查。
美国疾病控制与预防中心(CDC)顾问小组安排于周二举行会议,对哪些人应该接种更新版疫苗提供建议。
诺瓦瓦克斯首席执行官John Jacobs在接受采访时表示,公司预计其疫苗将在近期获得FDA授权。
Jacobs指出,诺瓦瓦克斯已做好准备,生产了数千万剂新疫苗,并签署了在全美范围内广泛分销的合同。
目前,因为新的新冠病毒变种不断出现并在全球传播,美国新冠病毒感染病例和住院人数有所上升,但远未达到大流行的水平。
尽管自2020年以来,美国每年出现两波新冠感染浪潮,分别在夏末和冬季中期,但FDA要求公司只在秋季准备疫苗推广,并在夏季投票决定针对哪种变体。
专家们一致认为,老年人、免疫功能低下者或有慢性健康问题的人更需要定期接种COVID-19强化疫苗。
本周晚些时候,美国将启动今年的秋季疫苗接种活动。
辉瑞和莫德纳表示,它们针对奥密克戎亚变体XBB.1.5病毒的更新版疫苗预计将在未来几天内向美国大多数人提供。
FDA批准这些疫苗用于12岁及以上人群,并授权其紧急用于6个月至11岁的儿童。
美国政府于今年5月终止了应对新冠疫情的公共卫生紧急状态,并将疫苗接种的责任移交给了私营部门。
目前,大多数有医疗保险的美国人仍可免费接种新冠疫苗。
美国政府也表示,正在制定一项计划,为没有保险的人免费提供疫苗。
主编精选,篇篇重磅,请点击订阅“邮件订阅”
评论
 |
|


